Ein Forschungsteam des Ulsan National Institute of Science and Technology (UNIST) in Südkorea hat kürzlich nachgewiesen, dass flüssige Elektrolyte auch im gefrorenen Zustand eine ausreichende Lithiumionenleitung zur Unterstützung des Batteriebetriebs aufrechterhalten können. Diese Entdeckung stellt die herkömmliche Ansicht in Frage, dass Elektrolyte flüssig sein müssen, um zu funktionieren. Die Studie enthüllt zudem den Transfermechanismus von Lithiumionen in organischen Eiselektrolyten und eröffnet neue Möglichkeiten für die Entwicklung von quasi-festen Elektrolyten für Lithiummetallbatterien. Die zugehörigen Ergebnisse wurden in der Fachzeitschrift „Advanced Materials“ veröffentlicht.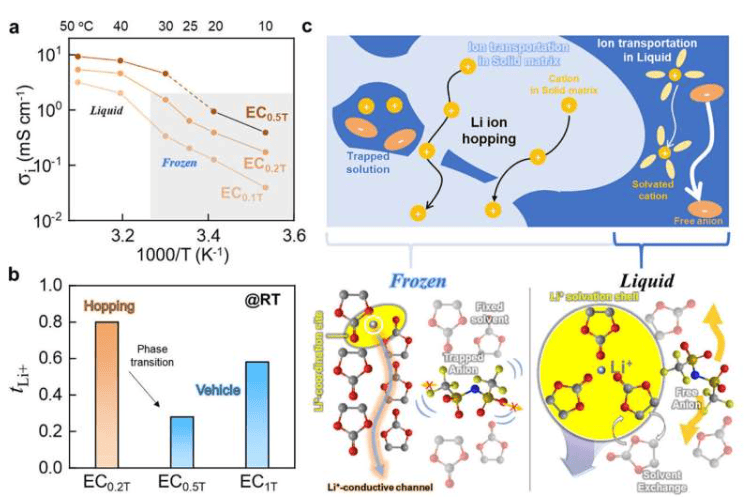
Diese Studie wurde gemeinsam von Prof. Hyun-Kon Song von der Fakultät für Energie und Chemieingenieurwesen der UNIST und Prof. Dong-Hwa Seo von der Fakultät für Materialwissenschaft und -technik des Korea Advanced Institute of Science and Technology (KAIST) geleitet. Das Team stellte organische Eiselektrolyte auf Basis von Ethylencarbonat her. Ethylencarbonat ist ein cyclisches Carbonat, das häufig in kommerziellen Batterien verwendet wird.
Das Forschungsteam testete die Ionenleitfähigkeit und die Lithiumionentransportefficienz der Elektrolyte im gefrorenen Zustand. Die Ergebnisse zeigen, dass diese Elektrolyte Ionenleitung durch einen Sprungmechanismus innerhalb einer festen Struktur aus immobilisierten Lösungsmittelmolekülen ermöglichen.
In herkömmlichen Lithiumionenbatterien ist der Elektrolyt eine flüssige Lösung aus Lithiumsalzen in organischen Lösungsmitteln, die es Lithiumionen ermöglicht, sich während des Lade- und Entladevorgangs zwischen den Elektroden zu bewegen. Ethylencarbonat hat einen Schmelzpunkt von etwa 37°C und ist daher bei Raumtemperatur (ca. 25°C) fest. Normalerweise muss sein Schmelzpunkt durch Beimischung anderer Lösungsmittel gesenkt werden. In dieser Studie wurde der Elektrolyt jedoch so konzipiert, dass nur eine geringe Menge Lithiumsalz hinzugefügt wurde, um ihn in einem gefrorenen, eisähnlichen Zustand zu halten.
Die experimentellen Ergebnisse zeigen, dass dieser „Eis-Elektrolyt“ eine Ionenleitfähigkeit von etwa 0,64 mS/cm und eine Lithiumionen-Überführungszahl von etwa 0,8 aufweist. Diese Werte sind mit denen einiger fortschrittlicher fester Elektrolyte vergleichbar. Bei Anwendung in einer Lithiummetallbatterie ermöglichte dieser gefrorene Elektrolyt bei Raumtemperatur über 400 Lade-Entlade-Zyklen ohne interne Kurzschlüsse und zeigte eine relativ stabile Leistung.
Lithiummetallbatterien gelten aufgrund ihrer um etwa 50 % höheren Energiedichte im Vergleich zu herkömmlichen Batterien als vielversprechende Energiespeicherlösung. Ihre Anwendung wurde jedoch bisher durch Probleme wie Dendritenwachstum eingeschränkt. Dendriten sind scharfe Lithiumablagerungen, die den Separator durchbohren und Kurzschlüsse verursachen können. Darüber hinaus begrenzen Nebenreaktionen zwischen dem Lithiummetall und dem flüssigen Elektrolyten seine Verbreitung.
Die Forscher analysierten den Leistungsmechanismus des Eiselektrolyten. Die Analyse zeigt, dass im gefrorenen Zustand die Lösungsmittelmoleküle immobilisiert sind und Lithiumionen durch Sprünge zwischen benachbarten Sauerstoffatomen gerichtet wandern. Dieser Mechanismus trägt dazu bei, Nebenreaktionen zu reduzieren und die Dendritenbildung zu unterdrücken.
Prof. Hyun-Kon Song erklärte: „Während viele glauben, dass feste Elektrolyte starre anorganische Materialien oder spezielle Polymere sein müssen, zeigt unsere Entdeckung, dass selbst lockere, eisähnliche Strukturen aus Lösungsmittelmolekülen eine effektive Ionenleitung unterstützen können. Wir erforschen derzeit organische Lösungsmittelkombinationen mit höheren Schmelzpunkten, um diesen Ansatz für praktische Anwendungen besser nutzbar zu machen.“
Veröffentlichungsdetails: Autoren: Do Sol Cheong et al., Titel: „Conduction of Lithium Ions in Frozen Phases of Organic Electrolytes“, veröffentlicht in: Advanced Materials (2026). Zeitschrifteninformation: Advanced Materials
