In zwei in der Zeitschrift Nature veröffentlichten Studien enthüllten Forschungsteams der Purdue University und der Columbia University ein natürlich entwickeltes Gen-Editing-System, das die Genexpression aktivieren kann und damit Vorteile gegenüber bestehenden CRISPR-Technologien bietet, die lediglich DNA schneiden. Die Forschung umfasst zwei komplementäre Arbeiten, die jeweils die biologische Funktion und den molekularen Mechanismus des Systems untersuchen.
Diese Studie erweitert das Verständnis der natürlichen Vielfalt von CRISPR-Systemen und bietet eine Grundlage für neue Technologien zur Genregulation. Diese CRISPR-Variante aktiviert Gene, ohne die DNA zu schneiden, und eignet sich für präzise Genkontrollanwendungen, einschließlich als Forschungswerkzeug und potenzielle therapeutische Strategie, ohne das Genom dauerhaft zu verändern.
Eine Studie zeigt, dass dieses CRISPR-System RNA als Leitfaden nutzt, um spezifische DNA-Regionen zu lokalisieren und den eigenen Genexpressionsmechanismus der Zelle anzuziehen, um Gene zu aktivieren. Eine andere Studie erklärt, wie der molekulare Komplex diese Aufgabe ausführt, indem Strukturanalysen zeigen, dass er RNA-Polymerase rekrutieren kann, um die Genexpression zu starten.
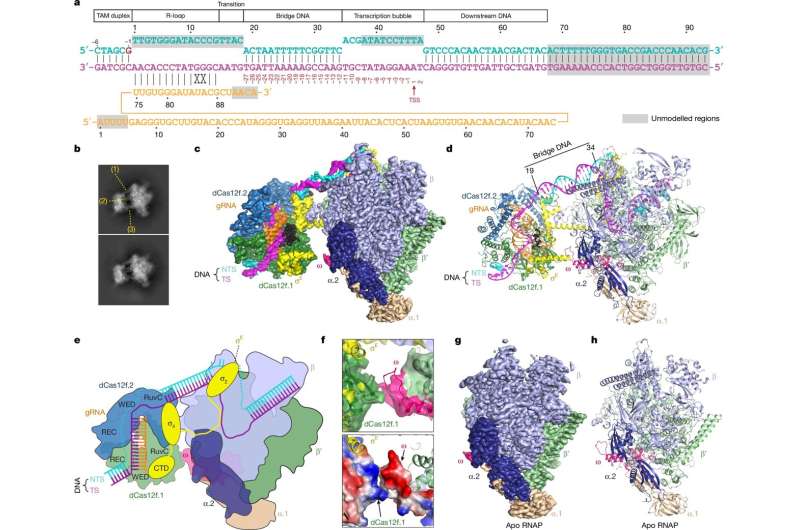
Unter der Assistenz von Postdoktorand Renjian Xiao und Doktorandin Dan Xie enthüllte Chang (Zhang) mittels Kryo-Elektronenmikroskopie und biochemischen Experimenten die Struktur und den Mechanismus des RNA-gesteuerten Genaktivierungssystems. Die Forscher visualisierten den Multiproteinkomplex mit nahezu atomarer Auflösung und zeigten, wie die RNA-Führung den Komplex zu bestimmten DNA-Sequenzen lenkt und ihn mit dem Transkriptionsmechanismus verbindet.
„Im traditionellen CRISPR führt die RNA den Komplex zur DNA-Zielstelle, um sie zu schneiden. Hier lenkt die RNA den Komplex immer noch zum Ziel, schneidet aber nicht mehr die DNA, sondern rekrutiert den Transkriptionsmechanismus der Zelle, um die Genexpression zu aktivieren“, sagte Chang. „Das ist wie der Wechsel von einer molekularen Schere zu einem GPS-gesteuerten Aktivierungsschalter.“

Die Studie fand auch heraus, dass das System die Transkription selbst an genomischen Positionen ohne Promotorsequenzen aktivieren kann, was die Vielfalt von CRISPR-Systemen in der Natur unterstreicht. Chang fügte hinzu: „Unser Ziel ist es, die grundlegenden Mechanismen RNA-gesteuerter molekularer Maschinen zu verstehen. Indem wir auf molekularer Ebene definieren, wie diese Systeme funktionieren, können wir die Grundlage für sicherere und funktionalere Technologien zur Genom-Editierung legen.“
Veröffentlichungsdetails: Autor: Alisha Willett, Purdue University; Titel: „RNA-guided CRISPR system activates gene expression“; veröffentlicht in: Nature (2026).
